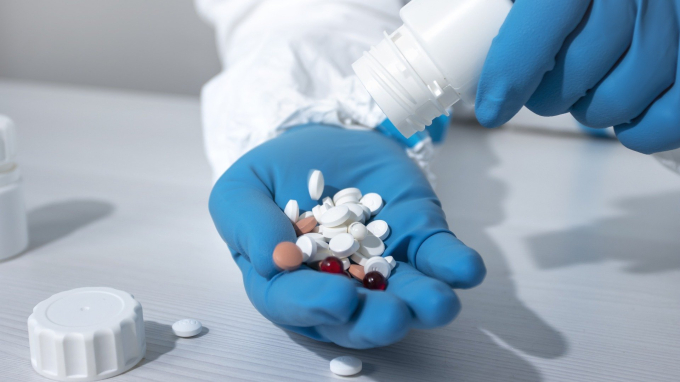
26일 업계에 따르면 그 동안 임상 문턱을 넘지 못한 치매 치료제가 FDA 승인을 받고, 잇따라 임상 2·3상에 들어선 사례가 나타나면서 치매 약물 탄생이 가시화되고 있다. 현재 시판 중인 도네페질, 갈란타민 등의 약물은 원인 치료제가 아닌 증상 완화에 그친다.
바이오젠의 ‘아두카누맙(상품명 아두헬름)’은 2021년 미국 FDA로부터 알츠하이머 치료제 조건부 승인을 받았다. 최초로 치매의 원인을 치료할 수 있는 가능성을 인정받은 셈이다.
아두카누맙은 뇌혈관에 쌓이는 ‘아밀로이드베타’라는 단백질을 제거해 병의 발병을 늦추는 단일 기전을 갖고 있다. 아밀로이드베타가 지나치게 쌓이면 신경 독성을 일으켜 기억력 저하, 언어능력 및 시공간 파악능력이 떨어진다.
하지만 해당 약물은 최근 안전성 및 유효성 문제가 불거지며 논란이 되고 있다. 미국 임상 3상 결과, 아두카누맙은 고용량 투약군에서만 인지기능을 개선 효과를 보였다. 문제는 고용량군에서 뇌염증 및 부종 등으로 인해 환자가 사망하는 사례가 발생했다는 점이다.
이에 따라 유럽의약품청(EMA)에서는 해당 약물의 허가 권고를 내리기 어렵다고 판단했고, 바이오젠도 허가신청을 자진 철회했다. 지난 7월 국내 식품의약품안전처에서도 허가 신청서를 검토했지만 ‘효능을 충족시키지 못한 해당 약물의 허가를 논의하는 것은 타당하지 않다’고 평가해 도입 난항이 예견된다. 현재 바이오젠은 추가적 효능 입증을 위한 국내외 임상 3·4상 준비에 돌입했다.
이와 관련 박기영 대한치매학회 기획이사는 “아두카두맙의 효과가 있냐고 물어본다면 ‘거의 없다’고 봐야 한다. 하지만 일부 케이스에서 원인 물질을 고용량으로 감소시켰다는 결과가 나왔고, 이제껏 그런 약제가 없었던 만큼 한 단계 도약한 계기가 됐다고 봐야한다”며 “이를 발판으로 후속 연구가 빛을 발할 것”이라고 언급했다.
김영수 연세대학교 약학과 교수는 “현재 진행되는 대부분 연구는 알츠하이머에서 나타나는 특징인 아밀로이드베타와 치매 유발 단백질인 타우 단백질을 타깃으로 한다”며 “해당 기전은 오랜 기간 연구에도 뚜렷한 결과를 보이지 못하고 있다. 또한 생산단가가 매우 높고 주사제로만 사용할 수 있다는 단점이 있다”고 설명했다.
이어 “최근엔 다중(multi) 기전을 타깃한 약물 개발이 늘고 있다. 다중 기전이란 아스피린과 같이 하나의 약으로 여러 효과를 내는 것을 말한다. 치매치료제 경우에는 아밀로이드베타·타우단백질 제거, 신경세포 시냅스 강화 등 여러 효과를 나타낸다”며 “이를 토대로 국내 바이오 업체들도 속속 임상에 진입하고 있다”고 언급했다.
아리바이오, 젬백스 등 결승선 다가가는 국내 바이오 업계
아리바이오는 다중기전 타깃 경구 치매치료제 ‘AR1001’을 개발 중이다. 지난 8일 미국 3상 임상 계획을 등재했고, 12월 본격적으로 임상을 시작할 예정이다.
펩타이드 등 저분자화합물을 기반으로 하면서도 다중기전을 갖는 바이오社도 있다. 젬백스앤카엘은 다중기전 치매치료제 ‘GV1001’의 전임상 단계를 지나 국내 3상 및 미국 2상에 들어갔다. 지엔티파마의 ‘크리스데살라진’은 국내 임상1상, 샤페론의 ‘누세린’은 국내 임상1상을 진행 중이다.
일동제약은 아밀로이드베타 기전에 신경세포 보호를 더한 치료제 ‘ID1201’ 임상3상 중이다. 메디포스트는 아밀로이드베타, 타우를 모두 타깃하는 줄기세포 기반 치매치료제로 미국 1·2a상을 시작하려 했지만 임상근거 미확보에 따라 임상을 보류하기로 했다.
업계 관계자는 “알츠하이머나 치매치료제 모두 병리와 증상을 동시에 잡기 어려워 개발이 힘들다. 인지기능 저하 정도를 임상효과 지표로 하는데, 약물로 이를 막는다고 해도 이미 파괴된 단백질이 남아있기 때문에 바로 좋아질 수 없다”며 “즉 임상기간이 길어야 약효를 볼 수 있다”고 설명했다.
이어 “따라서 국내 개발사들이 효과적으로 임상을 진행하고 결과를 도출하기 위해선 정부의 적극적인 지원이 필요하다”며 “국내 임상만으로도 해외에서 인정받을 수 있는 임상시험 인프라를 만들어주길 바란다”고 전했다.
박선혜 기자 betough@kukinews.com































































 포토
포토





![한 지붕 多 가족, 멀티 레이블의 함정 [데스크칼럼]](http://img.kukinews.com/data/kuk/image/2024/04/24/kuk202404240205.300x280.0.jpg)