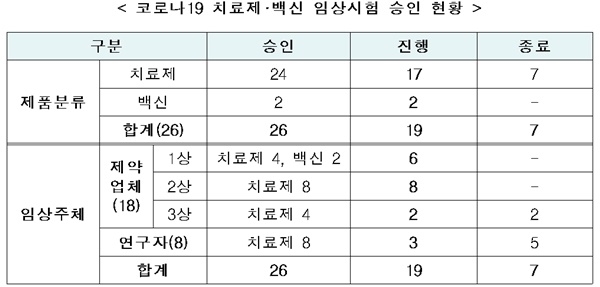
[쿠키뉴스] 유수인 기자 = 현재까지 국내에서 승인한 코로나19 관련 약물 임상시험은 치료제 24건, 백신 2건 등 총 26건으로 집계됐다. 이 가운데 치료제에 대한 임상시험 7건이 종료돼 현재 진행 중인 임상시험은 치료제 17건, 백신 2건으로 확인됐다.
식품의약품안전처는 전 세계적으로 코로나19 치료제 및 백신 개발이 활발히 진행되고 있는 가운데, 국내에서 개발되고 있는 코로나19 치료제·백신의 임상시험 및 허가·심사 현황에 대한 정보를 27일 공개했다.
현재 종료된 임상시험 7건은 렘데시비르(3건), 옥시크로린정·칼레트라정, 할록신정, 바리시티닙, 페로딜(각 1건) 등이다.
임상시험 중인 19건 중, 제약업체가 진행하고 있는 임상시험은 16건이며, 연구자가 진행하고 있는 임상시험은 3건이다.
제약업체가 진행하는 임상시험은 ▲1상 임상 6건(항체치료제, DNA백신 등) ▲2상 임상 8건(혈장분획치료제 등) ▲3상 임상 2건이다.
임상 1상은 최초로 사람에게 투여해 안전성, 약동학 등을 평가하는 단계이고, 1상 종료 후에는 임상 2상 단계로 넘어가 대상 환자들에게 투여해 치료효과를 탐색한다. 임상 3상은 2상 종료 후, 많은 환자들에게 투여해 안전성 및 치료효과를 확증하는 단계다.
치료제로는 항바이러스제, 중화항체치료제, 혈장분획치료제, 면역조절제가 개발 중이며, 부광약품(레보비르, 항바이러스제), 엔지켐(EC-18, 면역조절제), 신풍제약(피라맥스, 항바이러스제), 대웅제약(DWJ1248, 항바이러스제), 셀트리온(CT-P59, 중화항체치료제), 녹십자(GC5131, 혈장분획치료제) 등이 환자를 모집해 임상시험을 진행하고 있다.
백신은 제넥신(GX-19)이 환자를 모집해 임상시험을 진행하고 있다.
식약처는 코로나19 치료제·백신의 신속한 허가를 위해 운영 중인 ‘고(Go) 신속 프로그램’의 하나로, 허가신청이 예상되는 제품에 대해 신청 예정일로부터 90일 전에 ‘허가전담심사팀’을 구성하고 사전심사를 진행할 수 있도록 체계를 갖추었다.
현재 ‘아스트라제네카’에서 개발 중인 백신에 대해 허가전담심사팀을 구성해, 비임상 시험자료에 대한 사전검토를 시작했다.
한편, 식약처는 코로나19 백신의 신속한 임상시험 진입을 위해 지난 6월에 제정한 ‘코로나19 백신 개발 시 고려사항’을 개정했다.
주요 개정사항은 ▲3상 임상시험을 위한 자료요건 및 설계방법 ▲위해성관리계획 수립 등 시판 후 고려사항 ▲미국 FDA 등 외국 코로나19 백신 지침 추가 등이다. 위해성관리계획은 시판 후 부작용 조사를 위한 의약품 감시방법 및 위해성을 완화하기 위한 조치방법을 계획하고 실행하는 종합적인 시판 후 안전관리 활동이다.
식약처는 “코로나19 치료제·백신의 임상시험 등 개발 동향을 지속적으로 모니터링하고, 이를 바탕으로 국내 도입을 위해 필요한 품목허가, 특례제조·수입 등에 대한 사항을 지원하여, 우리 국민이 치료 기회를 보장받을 수 있도록 최선을 다하겠다”라고 전했다.
suin92710@kukinews.com




























