기초과학연구원(IBS)이 뇌졸중의 근본 원인을 규명하고 치료 가능성까지 입증하는 데 성공했다.
기초과학연구원(IBS) 이창준 기억및교세포연구단장팀과 을지대 유승준 교수팀이 뇌졸중 후유증을 일으키는 근본 원인을 규명하고 영장류 실험으로 자체 개발 신약 후보물질 치료 효과를 입증했다.
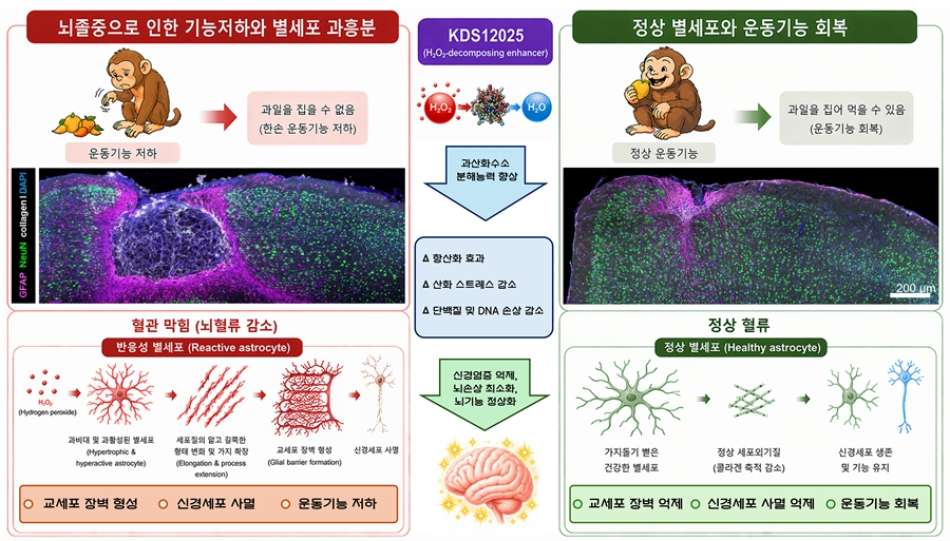
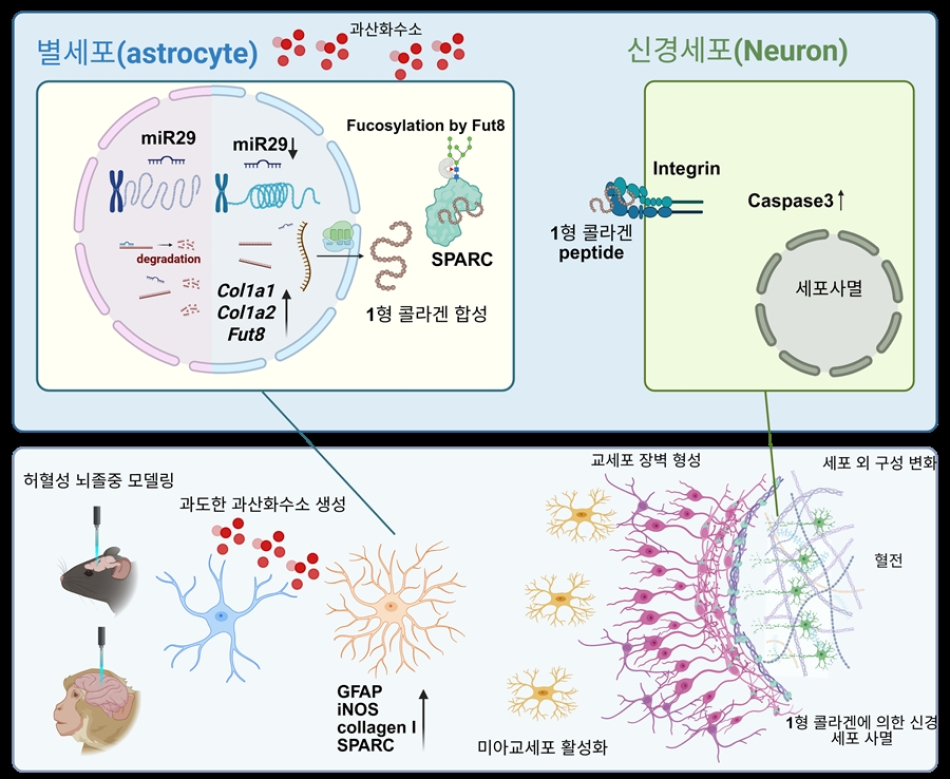
공동연구팀은 허혈성 뇌졸중 발생 이후 뇌에서 과산화수소가 급격히 증가하면 별세포가 1형 콜라겐을 생성, 신경세포를 사멸시킨다는 사실을 확인했다.
뇌에서 가장 많은 비중을 차지하는 별세포는 평소 뇌 환경을 안정적으로 유지하지만, 뇌졸중이 발생하면 손상 부위 주변에 교세포 장벽을 형성한다.
기존 학계는 이 장벽을 병변 확산을 막는 보호막으로 인식했다.
반면 연구팀은 이 장벽이 오히려 신경세포를 죽이는 원인이 된다는 점을 규명했다.
뇌졸중 직후 증가한 과산화수소가 별세포를 자극하면 별세포가 콜라겐을 분비하고, 이 단백질이 신경세포 표면 인테그린(integrin) 수용체와 결합해 세포 사멸을 유도했다.
분자세포 수준 분석 결과 별세포 내 콜라겐 생성은 마이크로RNA-29(miR-29)와 밀접하게 연관됐다.
평소 콜라겐 유전자를 분해하던 miR-29 농도는 뇌졸중 이후 낮아지면서 콜라겐 mRNA가 축적되고, 이후 당화과정을 거쳐 단백질 생성이 폭발적으로 늘었다.
연구팀은 뇌졸중 이후 세포 사멸까지 이어지는 전체 경로를 분자 축으로 연결해 규명하는 데 성공했다.
아울러 연구팀은 과산화수소를 제거하고 콜라겐 생성을 동시에 억제하는 신약 후보물질 'KDS12025'를 개발해 치료 가능성을 검증했다.
실험결과 생쥐 뇌졸중 모델에 약물을 투여하자 교세포 장벽 형성과 신경세포 사멸이 크게 줄고, 저하됐던 운동 기능도 일주일 만에 정상 수준으로 회복했다.
특히 뇌졸중 발생 2일이 지난 시점에 약물을 투여해도 신경 기능이 회복함으로써 기존 뇌졸중 치료의 한계인 골든타임을 획기적으로 확장할 근거를 마련했다.
이 같은 결과는 영장류 실험에서도 확실한 효과를 보였다.
뇌졸중으로 손이 마비된 원숭이에게 약물을 투여하자 3일 만에 병변 크기가 줄기 시작했고, 일주일 내로 마비된 손 기능을 완전히 회복했다.
실제 원숭이가 과일을 집어 먹는 행동 실험에서 치료받지 않은 원숭이는 움직일 수 없었지만, KDS12025를 투여한 원숭이는 10번 시도 모두 성공하며 인간과 생물학적으로 유사한 모델에서 임상 가능성을 강력히 입증했다.

이번 성과는 기초 메커니즘 규명부터 신약 개발, 전임상 검증까지 통합한 원스톱 연구 시스템 성과라는 점에서 의미가 크다.
특히 뇌졸중뿐 아니라 콜라겐 생성과 활성산소 불균형이 공통적으로 나타나는 치매, 파킨슨병 등 다양한 퇴행성 뇌 질환 치료에도 적용할 수 있을 전망이다.
이보영 IBS 기억및교세포연구단 연구위원은 “이번 연구는 별세포에서 활성산소에 의해 유도되는 콜라겐 합성 기전을 규명해 신경세포 사멸의 새로운 원인을 제시했다”고 설명했다.
유 교수는 “영장류 모델에서 치료 효과를 입증했기에 실제 환자 치료를 위한 임상 소요 기간을 대폭 줄일 수 있을 것으로 기대한다”고 말했다.
이 단장은 “기초연구를 통해 뇌졸중 근본 원인을 밝히고 구체적인 치료법까지 제시하는 데 성공했다”며 “KDS12025 사례처럼 인류와 사회에 직접 도움을 주는 연구를 지속하겠다”고 밝혔다.
한편, 이번 연구는 IBS 이재훈 선임연구원, 황인영 IBS 차세대 연구리더, 장현준 IBS 선임연구기술원이 제1저자로 참여했고, 연구결과는 28일 국제학술지 '셀 메타볼리즘(Cell Metabolism)' 온라인에 게재됐다.
(논문명: Oxidative stress-induced astrocytic collagen biosynthesis drives glial barrier formation and neuronal death in ischemic stroke
Cell Metabolism)







![[쿠키과학] 생명연 "유해조류 독성, 개체 수 아닌 성장 단계가 좌우"](/data/kuk/image/2026/05/07/kuk20260507000153.jpg)

![[쿠키과학] '침으로 PTSD 우울·불안 동시 완화'… 한의학연, 삼차신경 자극 침 치료](/data/kuk/image/2026/05/07/kuk20260507000124.png)